- Baza wiedzy
- Chirurgia
- Czy sto lat po odkryciu witaminy D istnieją dowody kliniczne nt. dawek suplementacji?
Czy sto lat po odkryciu witaminy D istnieją dowody kliniczne nt. dawek suplementacji?
Do czytelni
Artykuł przeglądowy
Autorzy: Ghanaati Shahram, Choukroun Joseph, Volz Ulrich, Hueber Rebekka, Mourão Carlos Fernando de Almeida Barros, Sader Robert, Kawase-Koga Yoko, Mazhari Ramesh, Amrein Karin, Meybohm Patrick, Al-Maawi Sarah
Artykuł został opublikowany w: International Journal of Growth Factors and Stem Cells in Dentistry
Rok wydania : 2020, tom: 3, numer: 1, strony: 3-11
Oryginalny artykuł, w formacie PDF zobaczyć i pobrać tutaj
Więcej o autorach znajdziesz tutaj
Tłumaczenie na język polski: FM Dental
Co znajdziesz na tej stronie:
- Abstrakt
- Wprowadzenie
- Pomiar stężenia witaminy D w surowicy i definicja hipowitaminozy
- Aktualne wytyczne dotyczące suplementacji witaminy D
- Suplementy witaminy D i dawki. Przegląd badań klinicznych
- Witamina D wspiera wrodzony i nabyty (swoisty i nieswoisty) układ odpornościowy
- Wpływ witaminy D na choroby przewlekłe
- Rola witaminy D w chorobach zakaźnych
- Jak suplementować witaminę D u osób dorosłych
- Uwagi końcowe i perspektywy na przyszłość
- Oświadczenia autorów nt. sponsoringu i konfliktu interesów
- O autorach
- Bibliografia
Abstrakt
Celem niniejszej pracy było przeglądowe przedstawienie dawek witaminy D podawanych w randomizowanych, kontrolowanych badaniach klinicznych, w celu oceny obecnie dostępnych dowodów klinicznych. Skupiono się na ostatnich postępach w zakresie badań nad działaniem witaminy D na obszary inne niż układ kostny. Wyniki czasami wskazywały na dużą rozbieżność zalecanej dawki witaminy D w zależności od organu regulacyjnego, gdzie wielkość dawki od 400 do 4000 IU / dobę, a dawki stosowane w ostatnich randomizowanych kontrolowanych badaniach klinicznych wynosiły nawet do 100 000 IU / dobę.
Różne badania wykazały pozytywny wpływ witaminy D na wsparcie układu odpornościowego i zapobieganie różnym chorobom przewlekłym i zakaźnym. Takie wynik wskazują na potrzebę ponownego przemyślenia zakresów dawek referencyjnych i zalecenia dotyczące spożycia.
Na podstawie analizowanego zakresu dawek stosowanych klinicznie zalecamy suplementację witaminy D w odniesieniu do trzech różnych zakresów, które obejmują <40 ng / ml,> 40 <80 ng / ml i> 80 ng / ml przy doustnym spożyciu witaminy D 10 000 IU / dzień, 5000 IU / dzień i Odpowiednio 1000 IU / dzień. Ponadto co 3 miesiące zaleca się monitorowanie poziomu 25-hydroksywitaminy D w surowicy krwi w celu ponownego dostosowania dawki witaminy D w oparciu o wyżej wymienioną koncepcję. Trwające badania kliniczne będą musiały dodatkowo udowodnić tę koncepcję dla różnych grup pacjentów.
Wprowadzenie
Zdrowy układ odpornościowy jest podstawą ogólnego zdrowia i obrony organizmu przed wieloma chorobami. Styl życia, indywidualne zachowania i środowisko życia mają bezpośredni wpływ na nasze zdrowie. W szczególności dobre odżywianie ma kluczowe znaczenie dla utrzymania ogólnego stanu zdrowia. (1) Brak równowagi i niedożywienie mogą zagrozić zdrowiu układu odpornościowego i zwiększają ryzyko chorób przewlekłych, którym można zapobiec. (1) W ostatnich dziesięcioleciach rozpowszechnienie chorób przewlekłych, takich jak cukrzyca, otyłość, choroby układu krążenia i nadciśnienie tętnicze znacznie wzrosło, zwłaszcza w krajach uprzemysłowionych. Jedną z najważniejszych przyczyn tej zmiany jest szybka zmiana stylu życia społeczeństwa. (2)
Rola witaminy D w zdrowiu i chorobach stopniowo zyskiwała coraz większe zainteresowanie w różnych dziedzinach. Witamina D została odkryta przez Adolfa Windhausa w 1922 roku, a w wkrótce potem (w r. 1928) Windhause otrzymał Nagrodę Nobla za badania nad sterolami i ich związkiem z witaminami (3), co zwiększyło zainteresowanie badawcze w tej dziedzinie.
Naturalnie endogenna synteza witaminy D zachodzi w skórze i jest ograniczona do czasu ekspozycji na słońce. Fale ultrafioletowe B przekształcają 7-dehydrocholesterolo cholekalcyferol (witamina D3). Witamina D, aby dotrzeć do formy aktywnej, ulega dalszym przemianom w wątrobie (do kalcydiolu 25-hydroksywitaminy D3 (25-OHD3)), która jest najbardziej wydajnym metabolitem witaminy D. Kolejny etap przemian zachodzi w nerkach, gdzie kalcydiol (25-OHD3) przekształca się w aktywną formę witaminy D, kalcytriol (1,25-dihydroksycholekalcyferol). Kalcytriol służy jako czynnik transkrypcyjny genów dla białek docelowych, a tym samym należy do szerokiej gamy hormonów. Dlatego witamina D jest uważana raczej za prehormon niż za witaminę (4,5) (Rysunek 1).
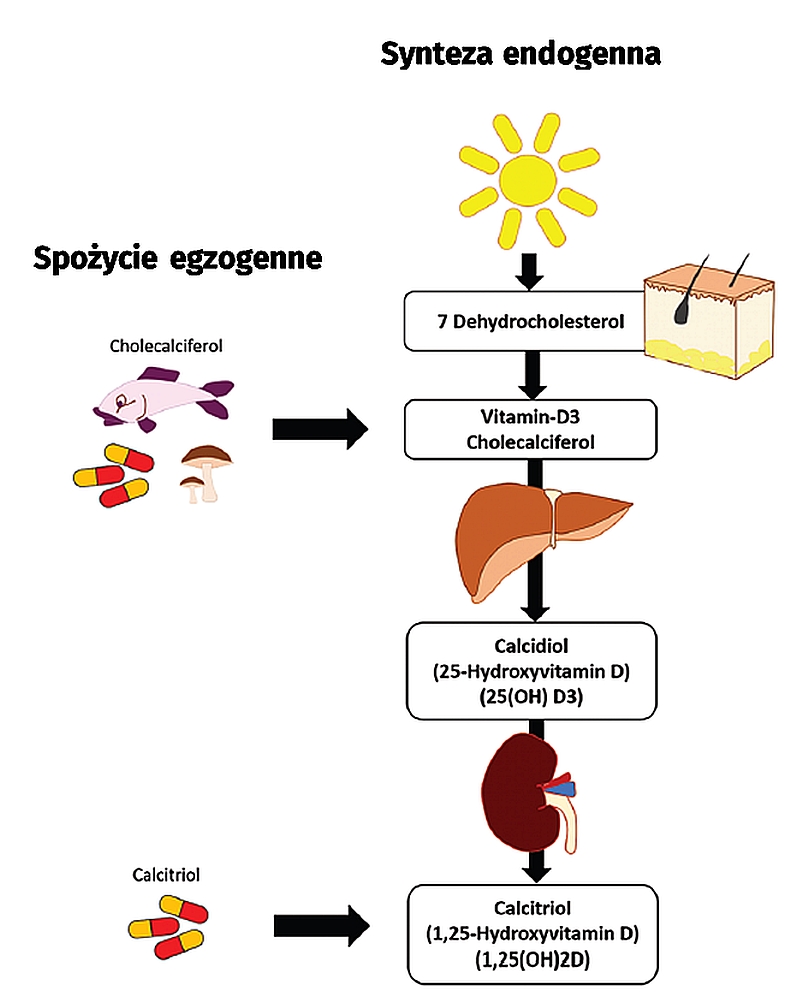
Rys. 1. Schematyczna ilustracja endogennej syntezy witamin oraz egzogennej aktywacji witaminy D
Wkrótce po odkryciu witaminy D został potwierdzony jej związek z parathormonem oraz rola witaminy D w regulacji hemostazy mineralnej i kostnej (6, 8). W tym procesie
aktywna postać witaminy D, czyli kalcytriol, wykorzystuje różne mechanizmy w celu utrzymania poziomu wapnia. Dodatkowo aktywuje formowanie i regenerację kości poprzez wsparcie różnicowania komórek i zwiększanie stężenia wapnia i fosforanów w surowicy. (9) Krzywica u dzieci jest jedną pierwszych z chorób, której mechanizm został dobrze zrozumiany właśnie dzięki odkryciu skutków niedoboru witaminy D. Podobnie było z osteomalacja u dorosłych, które to charakteryzują się poważnymi zaburzeniami mineralizacji. (10) Tym samym wiele badań skupiało się głównie na roli witaminy D dla zdrowia kości. Co więcej, witamina D zyskiwała coraz większe znaczenie w leczeniu pacjentów cierpiących na osteoporozę. Historyczne uwarunkowania odkrycia witaminy D sprawiły, iż stała się ona najbardziej popularna w odniesieniu do zdrowia układu kostnego.
W ostatniej dekadzie liczne badania wykazały, że witamina D odgrywa kluczową rolę w utrzymaniu ogólnego stanu zdrowia i wpływa na szereg funkcji organizmu. (9) W różnych badaniach donoszono o wpływie witaminy D na zapobieganie chorobom przewlekłym i zmniejszenie częstości występowania chorób układu krążenia i chorób metabolicznych, takich jak cukrzyca. (11) Ponadto w wielu badaniach analizowano wpływ witaminy D na układ odpornościowy i wykazano jej zdolność do zmniejszania stanu zapalnego i wspomagania regeneracji w różnych badaniach przedklinicznych i klinicznych. (12) W tym kontekście witamina D wykazała również korzystny wpływ na profilaktykę zakaźnych chorób bakteryjnych i wirusowych, takich jak grypa (13) i ostre zakażenia dróg oddechowych. (14) Witamina D odgrywa zarówno klasyczną rolę dla zdrowia kości i wykazuje przy tym immunologiczne działanie. Dlatego też należy podkreślić znaczenie konieczności jej odpowiedniego spożycia i utrzymania wymaganego poziomu w organizmie.
Niestety endogenna synteza witaminy D jest ograniczona ekspozycją na słońce, które w wielu krajach nie jest dostatecznie dostępne przez cały rok. Co więcej, spożycie egzogenne przez żywność jest ograniczone i raczej nieznane dla większości populacji świata. Czynniki te spowodowały w ostatnich latach częste występowanie niedoboru witaminy D w wielu różnych krajach. (15) Do tej pory pandemia niedoboru witaminy D była często odnotowywana, ale nie była dobrze rozpoznawana w wielu krajach. (16) Pierwsze rekomendacje mówiące o konieczności zalecania suplementacji witaminy D miały miejsce już 1940 roku. (17) Osiemdziesiąt lat później nadal nie ma konsensusu co do suplementacji i spożycia witaminy D. (17) Jednym z powodów takiego stanu rzeczy jest historyczny aspekt związany z odkryciem i zrozumieniem roli witaminy D. Zalecenia dotyczące suplementacji koncentrowały się głównie na spożyciu niezbędnym do utrzymania zdrowia kości. I chociaż notuje się coraz więcej dowodów na liczne funkcje witaminy D w zapobieganiu wielu chorobom, to wytyczne dotyczące suplementacji niewiele się zmieniły.
Dodatkowym czynnikiem są słabe dowody, które pozwoliłyby wskazać zakres stężeń witaminy D w surowicy zapewniający zdrowe funkcjonowanie organizmu. Nie ma również dobrych dowodów na maksymalny zakres stężeń, który należy zachować, biorąc pod uwagę wszystkie znane funkcje witaminy D. Aspekt stężeń witaminy D poruszany w literaturze był niespójny z powodu braku standaryzacji testów w clu pomiaru witaminy D, które były różne w zależności od laboratorium badawczego. (18) Ponadto istnieje wiele obaw dotyczących toksyczności witaminy D.
Ogólnie rzecz biorąc, z klinicznego punktu widzenia istnieje duża potrzeba zrozumienia roli witaminy D i zwrócenia uwagi współczesnych badaczy na ustanowienie protokołów suplementacji, których celem jest utrzymanie dobrego, ogólnego stanu zdrowia.
Niniejsza praca ma na celu ocenę aktualną ocenę dostępnych dowodów poprzez przedstawienie przeglądu podawanych dawek witaminy D w randomizowanych kontrolowanych badaniach klinicznych. Ponadto niniejszy przegląd skupia się na ostatnich postępach prac nad witaminą D w zakresie jej działania na funkcje organizmu nie związane z układem szkieletowym.
Pomiar stężenia witaminy D w surowicy i definicja hipowitaminozy
Witamina D (25-hydroksywitamina D (25 (OH) D)) cząsteczkową wysoko lipofilową. Podczas krążenia we krwi ok 80% witaminy D jest związane z białkiem nośnikowym ( en: DBP - D Binding Protein - białko wiążące witaminę D). Kolejne 10–15% witaminy D jest transportowane przez albuminę białka nośnikowego. Tylko niewielka część witaminy D krąży swobodnie we krwi i jej dostępność dla komórek jest wyższa. Stężenie 25 (OH) D w surowicy jest najbardziej wiarygodnym wskaźnikiem do oceny poziomu witaminy D. Jednak pomiar wolnego 25 (OH) D jest technicznie raczej trudny ze względu na niskie stężenie i ograniczenie dostępnych metod badawczych. (19) Ten aspekt jest nadal tematem dyskusji w badaniach. W rutynowej praktyce klinicznej w celu oceny poziomu witaminy D mierzone jest całkowite stężenie 25 (OH) D w surowicy. (15) Podobnie jak inne witaminy i składniki krwi, wartości witaminy D są najczęściej wyrażane w nanomolach na litr (nmol / l) lub w nanogramach na mililitr (ng / ml) zgodnie z używanym systemem jednostek. Zasadniczo 1 nmol / l równa się 0,4 ng / ml (przelicznik: 2,5).
W związku z różnymi zaleceniami zakresy referencyjne witaminy D nie są jednolite. Jednak najbardziej rekomendowany zakres witaminy D w surowicy, uznawany za odpowiedni i zdrowy wynosi zdrowy 40–60 ng / ml (100–150 nmol / l). (20)
W literaturze stężenie w surowicy poniżej 30 ng / ml (75 nmol / l) jest uważane za niedostateczne.(16,17,20,21) W wielu badaniach, wykonywanych w różnych populacjach, donoszono o niedostatecznym poziomie witaminy D, stąd można mówić o pandemii deficytu witaminy D. (16,22) Badania obserwacyjne wskazują, iż częstość występowania niskiego poziomu 25 (OH) D poniżej 20 ng / ml (50 nmol / l) osiąga 24% w USA, 37% w Kanadzie i 40% w Europie. (16,20) Takie poziomy są obserwowane na całym świecie, na przykład ponad 20% populacji Indii miało poziom 25 (OH) D poniżej 12 ng / ml (30 nmol / l). (16) Poziom stężenia 25 (OH) D w surowicy zależy od ogólnego stanu zdrowia, stylu życia, masy ciała i wieku.
INFORMACJA Z SERWISU FM DENTAL
Z najnowszych szacunków wykonanych w Niemczech (w Instytucie Roberta Kocha) wynika, iż u 58% badanych osób w wieku 18–79 lat stężenie witaminy D surowicy wynosi poniżej 20 ng / ml (50 nmol / l). (23) Z kolei w Chinach, wśród kobiet w wieku pomenopauzalnycm, w okresie zimowym, stężenie w surowicy wynosiło 14 ng / ml (35 nmol / l).
We Włoszech w okresie letnim, wśród mężczyzn, średnie 25 (OH) stężenie D sięgało około 33 ng / ml (82,5 nmol / l) i 20 ng / ml, a zimą zimą (50 nmol / l). (20)
W naszym ośrodku przeprowadzono badanie pilotażowe wśród personelu medycznego zespołu chirurgii szczękowo twarzowej, stomatologicznej i plastycznej twarzy z Uniwersytetu Goethego (Niemcy). Przetestowano 24 ochotników - 85,7% z nich miało poziom witaminy D poniżej 30 ng / ml, a 45,8% badanych miało poziom witaminy D poniżej 10 ng / ml (Rysunek 2).
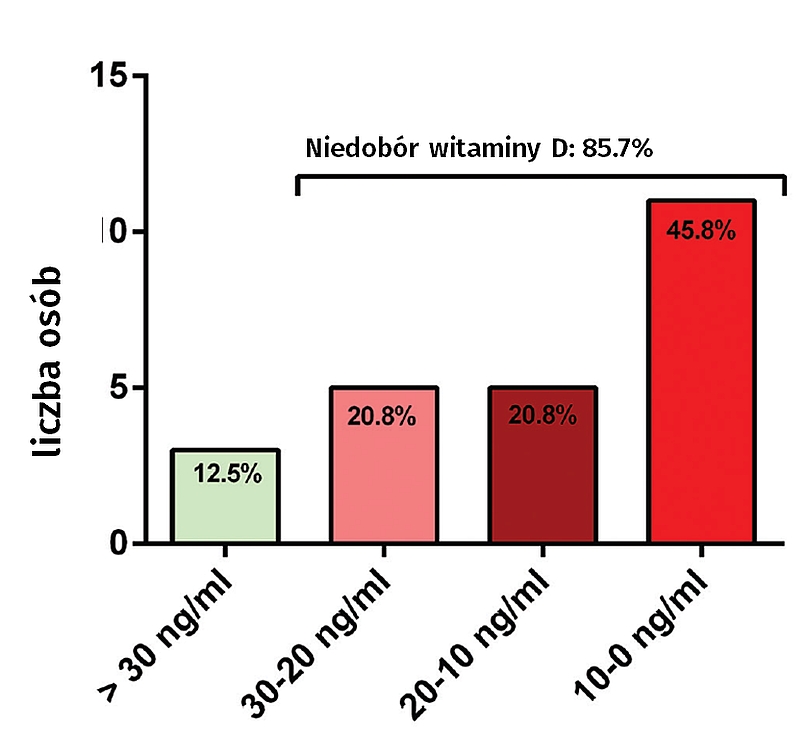
Rys.2 Poziom witaminy D zbadanych 24 ochotników - personelu medycznego chirurgii szczękowo twarzowej, stomatologicznej i plastycznej twarzy z Uniwersytetu Goethego (Niemcy).
Aktualne wytyczne dotyczące suplementacji witaminy D
Oprócz endogennej syntezy witaminy D istnieją również naturalne, egzogenne źródła witaminy D. Są to różnego rodzaju pokarmy. Zawartość witaminy D można wyrazić przy użyciu dwóch różnych jednostek, w zależności od używanego systemu. Jedną ze stosowanych jednostek jest masa w mikrogramach (μg). Alternatywnie stosowana jest jednostka międzynarodowa (IU), która jest najczęściej używana do określenia
ilości i dawek w suplementacji witaminy D. Ogólnie rzecz ujmując 40 IU to 1 μg.
Naturalnym źródłem suplementacji D może być żywność. Produkty pochodzenia zwierzęcego dostarczają głównie cholekalcyferol (witamina D3), natomiast roślinny i grzyby zawierają głównie ergokalcyferol (witaminę D2). (4) Najbogatszym naturalnym źródłem witaminy D są ryby. Przykładowo świeży węgorz dostarcza 1200 IU / 100 g ; świeży dziki łosoś zawiera do 1000 IU / 100 g, a pieczony łosoś dostarcza 540 IU / 100 g. (4) Jednak w większości przypadków wymagany poziom witaminy nie jest osiągalny z pożywienia (16) , dlatego suplementacja jest wysoce wskazana prawie w każdym przypadku. Z drugiej strony aktualne wytyczne dotyczące suplementacji są niespójne i oparte głównie na szacunkach, które uwzględniają tylko potrzeby układu szkieletowego. Zakres zalecanych pod tym kątem dawek wynosi od 400 IU / dzień do 4000 IU / dzień. Europejski Urząd ds. Bezpieczeństwa Żywności zaleca spożycie 600 IU / dzień dla w przypadku zdrowych, dorosłych osób. (24) Podobnie brytyjski Naukowy Komitet Doradczy ds Odżywiania zaleca spożycie 400 IU / dzień dla wszystkich grup wiekowych. (25)
Instytut Medycyny (USA) zaleca suplementację 600 IU / dzień na osoby w wieku poniżej 70 lat i 800 IU / dzień w przypadku osób powyżej 70 lat. (26) Niemieckie Towarzystwo Żywności w 2012 roku zaktualizowane zalecane wartości suplementacji i obecnie są inne dla różnych grup wiekowch. Dla niemowląt wynoszą one 400 IU / dzień, dla wszystkich innych grup zalecane spożycie to 800 IU witaminy D dziennie. (23) Amerykańskie Towarzystwo Endokrynologiczne zaleca stosowanie 1000–4000 IU / dzień. (27) Niektórzy autorzy zalecali dzienne spożycie 5000 IU / dzień do utrzymać zdrowy poziom witaminy D na poziomie około 40 ng / ml. (28) Instytut GrassrootsHealth zbierał dane dotyczące suplementacji w ilości dziennych dawek witaminy w wysokości 10000 IU / dzień i nie odnotował wystąpienia działań niepożądanych. (20,29,30)
Ponadto najwyższa tolerowana dawka potrzebna do osiągnięcia i utrzymania odpowiedniego poziomu witaminy D, bez wystąpienia efektu działania toksycznego i skutków ubocznych, pozostaje zmienna.
W oświadczeniu Europejskiej Agencji ds. Bezpieczeństwa Żywności (The European Food Safety Agency) czytamy, iż że dawki do 10 000 IU / dobę są bezpieczne dla pacjentów, którzy nie posiadają chorób współistniejących. Tymczasem Europejski Urząd ds. Bezpieczeństwa Żywności (European Food Safety Authority) uważa, że najwyższe bezpieczne dzienne spożycie wynosi 4000 IU / dobę. (24)
Suplementy witaminy D i dawki. Przegląd badań klinicznych
Oprócz zaleceń różnych światowych stowarzyszeń naukowych dostępne są dane z randomizowanych badań klinicznych (RCTs - randomized clinical trials). Badania te były przeprowadzane na wielu płaszczyznach klinicznych a ich celem było określnie protokołu suplementacji oraz wpływu witaminy D na osoby zdrowe oraz na pacjentów. (tab. 1).
Tabela 1: Przegląd podawanych dawek i stężeń w surowicy w wybranych badaniach klinicznych
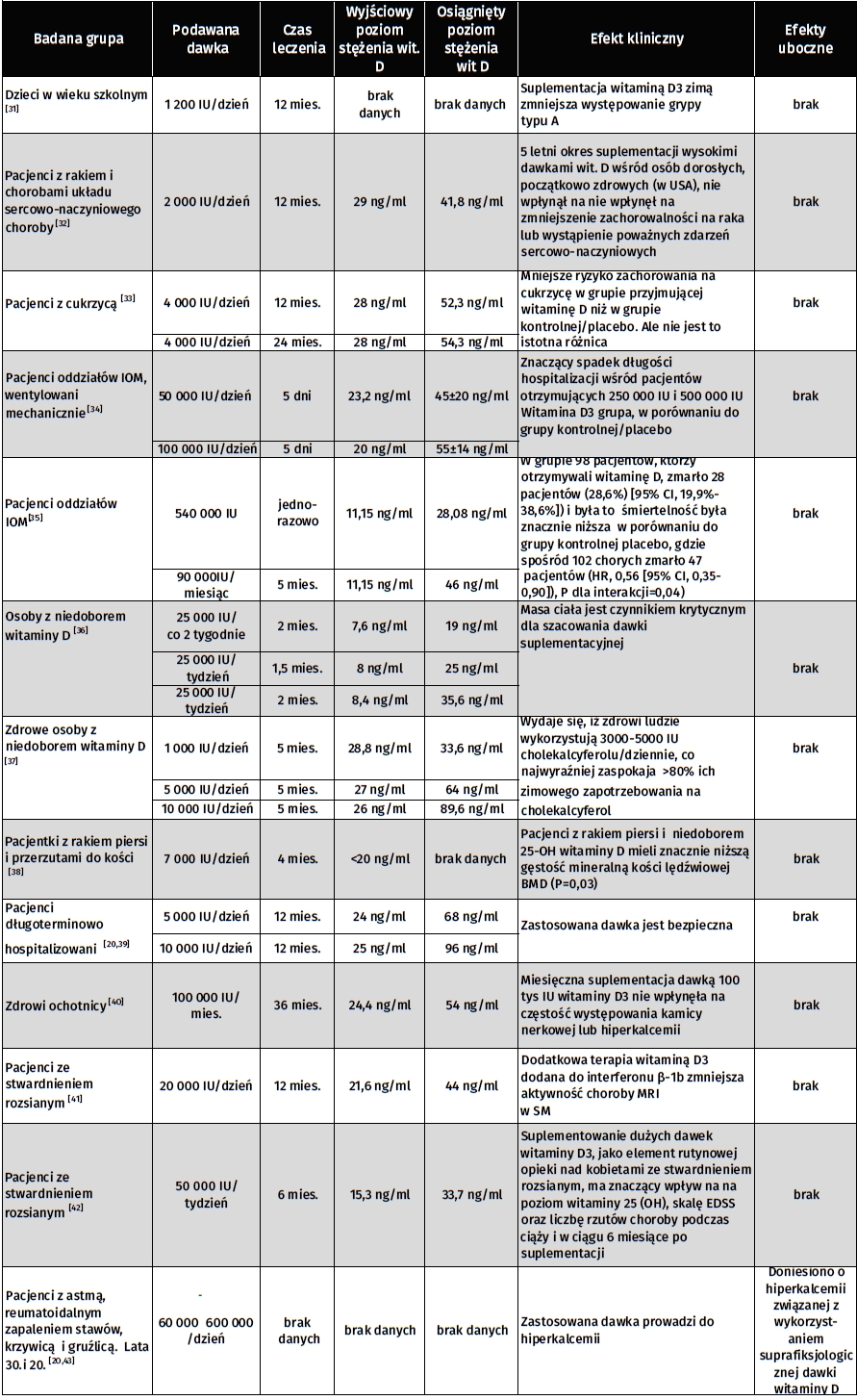
Tabela 1: Przegląd podawanych dawek i stężeń w surowicy w wybranych badaniach klinicznych
Dzieciom w wieku szkolnym w Japonii podawano 1200 IU witaminy D dziennie przez 1 rok, w ramach profilaktyki grypy. (31) Wyniki wykazały i znacznie zmniejszoną częstość występowania grypy wśród dzieci z grupy przyjmującej 1200 IU / dobę Witamina D. (31)
W badaniu VITAL przeanalizowano znaczenie witaminy D w profilaktyce raka i chorób układu sercowo-naczyniowego choroby. W badaniu tym wzięło udział łącznie 25 871 uczestników. Uczestnicy w grupie objętej suplementacją otrzymywali dawkę 2000 IU / dzień przez 5 lat. Niestety niedobór witaminy D nie stanowił kryterium włączenia uczestnika do tego programu badawczego. W tym długoterminowym badaniu nie odnotowano zdarzeń niepożądanych. (32)
W badaniu D2D (pacjenci diabetologiczni) osoby ze stanem przedcukrzycowym otrzymywały 4000 IU / dobę przez 2 lata, w celu podniesienia poziom witaminy D z 28 ng / ml do 54 ng / ml. Tutaj, również nie odnotowano toksycznego efektu działania witaminy D ani zdarzeń niepożądanych. (33)
Kolejne randomizowane badanie kliniczne obejmowało leczenie stosunkowo wysokimi dawkami stosowano u pacjentów oddziałów intensywnej terapii, którzy byli poddawani wentylacji mechanicznej.
Jedna grupa tych pacjentów otrzymywała dawkę 50 000 IU / dzień, podczas gdy druga grupa otrzymywała 100 000 IU / dzień. Taka suplementacja trwała 5 dni. Zlikwidowano niedobór witaminy D, a pacjenci osiągnęli poziom odpowiednio 45 ng / ml i 55 ng / ml. Nastąpiło znaczne skrócenie czasu hospitalizacji w grupach, które przyjęły 250 000 IU i 500 000 IU witaminy D3, w porównaniu z grupą placebo (25 ± 14 i 18 ± 11 dni w porównaniu do odpowiednio 36 ± 19 dni; P = 0,03). W badaniu nie wykazano żadnych zdarzeń niepożądanych związanych z witaminą D. (34)
INFORMACJA Z SERWISU FM DENTAL: Zobacz, jak działa mobilny system do badania poziomu witaminy D, który możesz wykorzystać w swoim gabinecie:
W innym badaniu zastosowano jednorazową suplementację 540 000 IU u pacjentów oddziały intensywnej terapii będących w stanie krytycznym. Następnie pacjenci otrzymywali miesięczną dawkę 90 000 IU w celu utrzymania poziom witaminy D.
Pierwotnym, końcowym badanym parametrem była długość pobytu w szpitalu. Mediana (przedział międzykwartylowy (IQR)) długości pobytu w szpitalu nie różniła się istotnie
między grupami (20,1 dni (IQR, 11,1–33,3) dla witaminy D3 vs. 19,3 dni (IQR, 11,1–34,9) dla placebo; P = 0,98). Śmiertelność szpitalna była znacznie niższa i wyniosła 28 zgonów
wśród 98 pacjentów (28,6% (95% przedział ufności (CI), 19,9% –38,6%)) dla witaminy D3 w porównaniu z 47 zgonami wśród 102 pacjentów (46,1% (95% CI, 36,2% –56,2%)), którzy otrzymali placebo (współczynniki ryzyka (HR), 0,56 (95% CI, 0,35–0,90), P dla interakcji = 0,04) ale nie śmiertelność 6 w okresie 6 miesięcznym (34,7% (95% CI, 25,4% –45,0%) dla witaminy D3 vs. 50,0% (95% CI, 39,9% –60,1%] dla placebo; HR, 0,60 (95% CI, 0,39–0,93), P dla interakcji = 0,12). (35)
Kolejne badanie analizowało dawki i okresy leczenia dla witaminy D w grupie wolontariuszy z niedoborem tej witaminy. Jedna grupa badanych otrzymała 25 000 IU co dwa tygodnie (dawka dobowa: 6250 IU / dzień) przez 2 miesiące, druga grupa otrzymywała 25 000 IU / tydzień (dawka dobowa: 3771 IU / dzień) przez 1,5 miesiąca, a trzecia grupa otrzymywała 25 000 IU / tydzień (dawka dobowa: 3771 IU / dzień) przez 2 miesiące. Wykazano, że suplementacja witaminy D raz na tydzień skutkowała uzyskaniem wyższego poziomu witaminy D w porównaniu do suplementacji w odstępach dwutygodniowych. W tym badaniu także nie zgłaszano zdarzeń niepożądanych. (36)
Celem kolejnego badania było określenie protokołu suplementacji. Badaniem zostali objęci pacjenci, u których zdiagnozowano niedobór witaminy D. Zostali podzieleni na grupy, które otrzymywały przez 5 miesięcy następujące dawki: 10001000 IU / dobę, 5000 IU / dobę, 10000 IU / dobę. Największy wzrost poziomu witaminy D został osiągnięty u pacjentów otrzymujących 10000 / dobę, przy czym nie odnotowano u tych pacjentów efektów działania toksycznego ani innych skutków ubocznych. (37)
Żadnych komplikacji (od red: związanych z suplementacją wit.D) nie odnotowano również wśród pacjentek z rakiem piersi z, przerzutami do kości, leczonych bisfosfonianami, i otrzymujących 7000 IU / dzień przez 4 miesiące.(38)
Inne badanie kliniczne (RCT) skupiało się na zdarzeniach niepożądanych związanych z nerkami. W tym badaniu uczestnicy otrzymywali duże dawki miesięczne 100 000 IU / miesiąc (obliczona dawka dobowa: ok 3000 IU / dzień) przez kilka lat. Wśród uczestników odnotowano 18 przypadków kamicy moczowej. 7 z nich odnotowano w grupie przyjmującej witaminę D, a 11 w grupie przyjmującej placebo. Ponadto w grupie przyjmującej witaminę D nie odnotowano przypadku hiperkalcemii. Autorzy doszli do wniosku, że tak wysoka dawka nie zwiększają ryzyka kamicy nerkowej. (40)
Historyczne badania nad wysokimi dawkami witaminy D przeprowadzone zostały w latach 30. i 40. XX wieku. Stosowano dawki dzienne od 60 000 IU / dzień i 600 000 IU / dzień w leczeniu różnych schorzeń, takich jak krzywica, astma, reumatoidalne zapalenie stawów i gruźlica. Badania te wykazały hiperkalcemię związaną z wysokimi dawkami witaminy D, która prawdopodobnie była związana z idiopatyczną hiperkalcemią dziecięcą spowodowaną utratą funkcji w wyniku mutacji CYP24A1. (20,43)
Witamina D wspiera wrodzony i nabyty (swoisty i nieswoisty) układ odpornościowy
Ocena wpływu witaminy D na układ odpornościowy budzi rosnące zainteresowanie. Kilka badań skupia się właśnie na tym aspekcie działania witaminy D na różne typy komórek. Receptor witaminy D jest obecny w wielu różnych komórkach ludzkiego ciała, w tym komórkach układu odpornościowego. Ten specyficzny dla witaminy D receptor należy do grupy receptorów jądrowych, które służą jako czynniki transkrypcyjne. Witamina D wiąże się z receptorem, a następnie reguluje ekspresję różnych genów i syntezę białka.
Szeroka obecność receptora witaminy D w organizmie świadczy o jego znaczeniu i wielofunkcyjnej roli. (9) Niedawno doniesiono o szczególnym aspekcie immunomodulacyjnym. W tym kontekście witamina D jest w stanie wzmocnić wrodzony układ odpornościowy i hamować nabyty (adaptacyjny) układ odpornościowy. (9)
Wiadomo, że komórki dendrytyczne i makrofagi jako część wrodzonej odporności układu, oraz limfocyty T i B jako część układu adaptacyjnego układu odpornościowego, wykazują ekspresję receptora witaminy D. W tym kontekście witamina D może regulować proces zapalny. (44) Kalcytriol, aktywna forma witaminy D, reguluje początkowy stan zapalny poprzez hamowanie proliferacji monocytów i indukcję różnicowania monocytów w makrofagi. Jednocześnie kalcytriol wzmacnia zdolność obronne makrofagów i wspiera ich funkcję fagocytotyczną i przeciwbakteryjną. Ponadto okazało się, że kalcytriol zmniejsza odpowiedź prozapalną komórek prezentujących antygen poprzez zmniejszenie ich zdolności do ekspresji cytokin prozapalnych, takich jak interleukina (IL) -1, IL-6, IL-12 i czynnik martwicy nowotworów-alfa. (5) Innym znaczącym efektem działania witaminy D jest hamowanie proliferacji limfocytów B i T oraz modulacja różnicowania fenotypów limfocytów T. Poprzednie badania wykazały, że witamina D hamuje wytwarzanie prozapalnych cytokin limfocytów Th1 i sprzyja ekspresji przeciwzapalnej cytokin limfocytów Th2, co dodatkowo wyjaśnia ich rolę jako immunomodulator. Ponadto wpływ witaminy D ma na komórki Trega okazał się zależny od stężenia. (9)
Kilka badań wykazało, że witamina D wykazuje zdolność do kontrolowania genów odpowiedzialnych za proliferację. Ten fakt podkreśla znaczenie witaminy D w profilaktyce raka i w terapiach wspomagających.
Badania kliniczne wykazały pozytywny wpływ witaminy D na zmniejszenie częstości występowania i wsparcie w leczeniu różnych typów raka, w tym raka piersi, okrężnicy, raka kolczystokomórkowego (SCC) i innych. (11)
Różne badania sugerowały, że witamina D ma również działanie antyproliferacyjne i proapoptotyczne na raka podstawnokomórkowego i komórki raka SCC, ale nie na zdrowe keratynocyty. (45)
Wpływ witaminy D na choroby przewlekłe
W ostatniej dekadzie odnotowano coraz częstsze występowanie różnych chorób przewlekłych, takich jak nadciśnienie, cukrzyca, choroby sercowo-naczyniowe i choroby autoimmunologiczne. Związek witaminy D w etiologii, profilaktyce i leczeniu chorób przewlekłych sugerowano w wielu badaniach klinicznych. Niedawno opublikowana metaanaliza przeprowadzona na 25 prospektywnych badaniach kohortowych z udziałem około 10000 przypadków wykazała wzrost ryzyka chorób sercowo-naczyniowych o 44% (RR = 1,44, 95% CI: 1, 24–1, 69) przy niskim poziomie witaminy D. Deficyt witaminy D zwiększa również ryzyko śmiertelności związanej z chorobami układu krążenia (RR = 1,54, 95% CI: 1,29–1,84) oraz zapadalność na te choroby (RR = 1,18, 95% CI: 1–1,39). (46)
Korelacja między poziomem witaminy D w surowicy a ciśnieniem krwi została przeanalizowana w badaniu klinicznym z udziałem 8155 pacjentów z nadciśnieniem i niedoborem witaminy D. Pacjenci byli zmotywowani do zwiększenia poziomu witaminy D do zakresu 40–60 ng / ml (100–150 nmol / l). Otrzymywali indywidualne dawki 1000–20 000 IU / dobę. Po 12 miesiącach 71% suplementowanych pacjentów nie miało już nadciśnienia. (47) Podobny efekty obserwowano w zapobieganiu i leczeniu cukrzycy.
Przeprowadzono również badanie na pacjentach z cukrzycą typu II i objawami depresji - od łagodnych do umiarkowanych. W tym badaniu wyodrębniono kontrolną grupę placebo. Grupa otrzymująca witaminę D spożywała 4000 IU / dzień. Poziom witaminy D wzrósł w tej grupie od 15,5 ± 8,8 ng / ml do 32,2 ± 8,9 ng / ml, a objawy depresyjne znacznie się zmniejszyły w porównaniu z grupą kontrolną. Ponadto średni poziom insuliny był istotnie wyższy w odpowiedzi na leczenie witaminą D w porównaniu z grupa kontrolna. (48)
Istnieją również dowody na korzystne działanie witaminy D w przewlekłej obturacyjnej chorobie płuc (POChP). Metaanaliza wykazała, że niedobór witaminy D wiązał się ze zwiększonym ryzykiem wystąpienia POChP (iloraz szans [OR]: 1,77, 95% CI: 1,18, 2,64, P = 0,006) oraz z ciężkim przebiegiem POChP (OR: 2,83, 95% CI: 2,00, 4,00, p <0,001). (49)
Choroby przewlekłe, takie jak reumatoidalne zapalenie stawów również związane są z niedoborem witaminy D. Jednak brak jest dostępnego konsensusu w sprawie protokołu suplementacji, a tym samym wyniki kliniczne nie są odtwarzalne. (50) Ponadto zwraca się uwagę na rolę witaminy D w chorobach autoimmunologicznych takie jak stwardnienie rozsiane (5,51)
Rola witaminy D w chorobach zakaźnych
Immunomodulacyjna funkcja witaminy D i jej wpływ na układ odpornościowy wskazuje na potencjalną rolę obronną tej witaminy w chorobach zakaźnych. Tymczasem wzrastało zainteresowanie wpływem poziomu witaminy D na zapadalność i występowanie chorób zakaźnych. Potencjał przeciwinfekcyjny tej witaminy sprawił, iż jest ona dobrym kandydatem do leczenia uzupełniającego w wielu chorobach zakaźnych. (13,52) W przeglądzie systematycznym zwrócono uwagą na korelację między niedoborem witaminy D a stanem pacjentów z przewlekłym wirusowym zapaleniem wątroby typu B. Ponadto wykazano, że niski poziom witaminy D wiąże się z wysokim mianem wirusa zapalenia wątroby typu B. (21)
Inne badania wykazały, że warianty genetyczne w szlaku metabolicznym witaminy D są zaangażowane w zakażenie wirusem zapalenia wątroby typu C. (53)
Ostatnie badania sugerowały również, że witamina D może hamować zakażenie opryszczką w komórkach nabłonka jamy ustnej poprzez regulację ekspresji genów cząsteczek obronnych, takich jak LL-37. (54)
Ponadto w kilku badaniach odnotowano pozytywny wpływ witaminy D na pacjentów zakażonych wirusem niedoboru odporności u ludzi.(55) Inne badania sugerowały, że mikroRNA regulowane przez witaminę D mogą mieć ochronny wpływ na zakażenie wirusem dengi.(56,57) W innym badaniu wykazano, że chorzy, u których wystąpiło zapalenie płuc, wykazywali znacznie niższy poziom witaminy D niż grupa zdrowa.(58)
Co ciekawe, w niedawnej metaanalizie wykazano polimorfizm receptora witaminy D, który koreluje z ryzykiem zakażeń wirusowych.(59)
Na podstawie tych danych w niedawno opublikowanym przeglądzie omówiono potencjalną rolę witaminy D w obecnej pandemii COVID-19, ponieważ wirus ten należy również do rodziny wirusów z otoczką .(20) Europejska Agencja Bezpieczeństwa Żywności stwierdziła, że dzienne dawki witaminy D do 10 000 / U są bezpieczne.(24)
Jak suplementować witaminę D u osób dorosłych
W literaturze donoszono o różnych dawkach stosowanych w celu uzyskania witaminy D na odpowiednim, zdrowym poziomie. Warto zauważyć, że wielu autorów zalecało wyższą dawkę dzienną niż oficjalne wytyczne władz czy insytucji, które to wytyczne w większości dotyczyły zdrowia kości. Jednak wiele badań dowiodło lub zasugerowało ważną rolę witaminy D w zdrowiu pozaszkieletowym.
Opierając się na wynikach tego przeglądu, sugerujemy codzienną suplementację odpowiednią dawką zamiast suplementację dużą dawką w odstępach czasowych. (60)
Badanie kliniczne wykazało, że po zwiększeniu poziomu witaminy D do wymaganej wartości, dzienna dawka suplementacji 2000 IU była niewystarczająca do utrzymania wymaganego poziomu witaminy D przez dłuższy czas. (61)
Zalecamy zindywidualizowaną dzienną dawkę witaminy D w zależności od potrzeb pacjenta. Poziom witaminy D <40 ng / ml wymaga dziennego spożycia 10 000 IU, aby szybko zwiększyć poziom do 40–80 ng / ml. Dawka ta została dokładnie zbadana i wykazano, że jest bezpieczna. (20,24,29,30)
Aby utrzymać prawidłowy poziom witaminy D (40–80 ng / ml), zalecamy dzienną dawkę 5000 IU. W przypadku przekroczenia zalecanego poziomu 40 i 80 ng / ml dzienne spożycie witaminy D należy zmniejszyć do 1000 IU. Wreszcie, 25 (OH) D powinno być monitorowane co 3 miesiące w celu oceny indywidualnych różnic w metabolizmie witaminy D i umożliwienia dalszego indywidualnego dostosowania dawki w zależności od potrzeb pacjenta (ryc. 3).
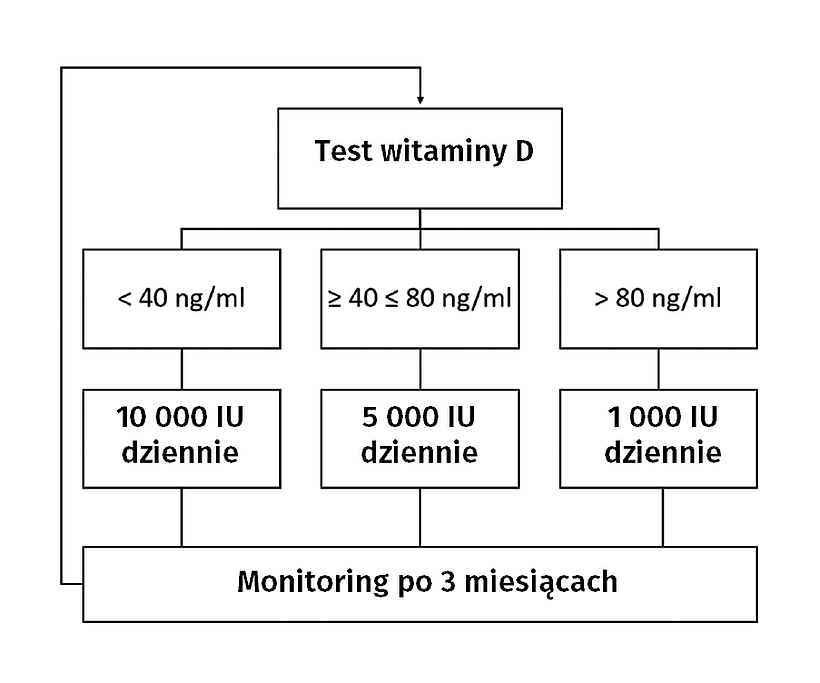
Rysunek 3. Protokół suplementacji witaminy D u zdrowych osób dorosłych, mający na celu utrzymanie odpowiedniego poziomu witaminy D.
Uwagi końcowe i perspektywy na przyszłość
Ostatnio witamina D zyskuje coraz większe zainteresowanie w różnych dziedzinach. W niniejszym przeglądzie nakreślono działania witaminy D nie związane z układem szkieletowym. Przedstawiono również przegląd aktualnych zaleceń suplementacji wydanych przez różne instytucje oraz zaprezentowano obecnie stosowane dawki suplementacyjne w badaniach klinicznych. Większość wytycznych zaleca codziennie dawki od 400 do 4000 IU / dobę. Ta duża zmienność zalecanych dawek jest zależna od uwarunkowań klinicznych, populacji objętej suplementacją i kraju. Jednak w badaniach klinicznych stosowano dawki do 100 000 IU / dzień i nie odnotowano toksycznego efektu działania witaminy D ani niepożądanych działań ubocznych.
Te wyniki ukazują ogromną rozbieżność pomiędzy rosnącymi dowodami w dziedzinie klinicznej i zalecaniami dotyczącymi dziennego spożycia. Jedną z przyczyn tej rozbieżności jest fakt, iż funkcje witamina D dla zdrowia innych układów niż kostnoszkieletowy nie były przez długi czas dobrze rozpoznane. Tym samym instytucje i badacze skupiali się zaleceniach głównie dotyczących dawek potrzebnych dla zdrowia układu kostnego. Niestety, pomimo rosnących dowodów na rolę witaminy D w funkcjonowaniu układu odpornościowego i w profilaktyce różnych chorób, większość zaleceń nie uległa zmianie.
Dodatkowo ciekawym wynikiem niniejszego przeglądu jest odnotowanie rozbieżności w odniesieniu do zakresu referencyjnego i hipowitaminozy. Powodem tej rozbieżności są zmienne techniki pomiarowe. W ostatnich latach podjęto wiele wysiłku w celu ustanowienia znormalizowanych metod pomiarowych z odpowiednimi referencjami. Badania, których celem jest umożliwienie powtarzalności i porównywalności wartości pomiaru na całym świecie są niezwykle potrzebne. Niektóre badania wykazały wcześniej, że ocena retrospektywna wartości witaminy D mierzonych za pomocą poszczególnych testów pokazała zupełnie inne wyniki przy użyciu standardowych referencji. (15) Ujednolicona ocena stanu witaminy D pozwoli na dokładniejsze zdefiniowanie niedoboru tej witaminy D.
Chociaż toksyczność witaminy D jest rzadka, to istnieją poważne obawy kliniczne dotyczące bezpieczeństwa dawki. Dla endogennej witaminy D syntezowanej przez skórę istnieje system ujemnego sprzężenia zwrotnego, podczas gdy żaden taki mechanizm regulacji nie jest dostępny dla wchłaniania egzogennego. Z tego powodu w przeszłości zgłaszano, że może to spowodować przedawkowanie witaminy D, hiperkalcemię lub kamienie nerkowe. Jednak bezpieczna maksymalna dawka nie została jeszcze zdefiniowana. Co więcej, nie ma żadnych dowodów łączących spożycie witaminy D z długotrwałym niekorzystnym skutkiem zdrowotnym.(17)
Badania kliniczne wykazały, że stosowanie dziennej dawki 20000 IU / dobę w okresie dłuższym niż 12 miesięcy było bezpieczne i nie powodowało niepożądanych, niekorzystnych działań ubocznych. (41)
W literaturze odnotowano kilka doniesień o zatruciu witaminą D. (43,62,63) Głównymi powodami tych doniesień były nieporozumienia w kwestii jednostek suplementacji witaminy D oraz pomylenie mikrogramów i jednostek międzynarodowych. Na przykład producent nie określił jasno dawki witaminy D w produkcie. Pacjenci, którzy przyjmowali np. dziennie 2 łyżeczki produktu dziennie sądzili, że przyjmują witaminę D w wysokości 2000 IU, a tymczasem otrzymali więcej niż 1 milion IU jednostek dziennie, przez ponad rok. (62,63) Inny przypadek to błędne obliczenie poziomu witaminy D w mleku wzbogaconym w tę witaminę - (250 000 IU w 8 uncji mleka), gdzie niektórzy konsumenci mieli poziom wapnia w surowicy około 16 mg / dl i poziom witaminy D około do 550 ng / ml. (64) Dawki notowane w tych przypadkowych zatruciach są znacznie wyższe niż wysokie dawki w przedstawionych tutaj protokołach klinicznych suplementacji. Te obserwacje dostarczają dobrze udokumentowane dowody zakresu wartości, przy których dochodzi do toksycznego działania witaminy D. Zalecając suplementowanie witaminy D należy mieć na uwadze, że nie ma predysponujących chorób współistniejących, które wpływają na metabolizm witaminy D lub niewydolność wątroby/nerek w tym zakresie.
W tym kontekście spersonalizowana dawka może być korzystna dla niektórych pacjentów w zależności od ich stylu życia, metabolizmu, i aktualnego poziomu witaminy D. Na przykład wielu pacjentów z zespołami złego wchłaniania aby osiągnąć odpowiedni zakresu witaminy D wymaga znacznie większej dawki suplementacji niż osoby zdrowe. (1,15)
Kolejnym czynnikiem, który, jak wykazano, ma wpływ na poziom witaminy D to masa ciała. Niedawne badanie wykazało, że poziom witaminy D wzrasta u osób z normalnym wskaźnikiem masy ciała (BMI). U tych osób poziom ten jest istotnie wyższy niż u tych, których wskaźnik BMI wynosi > 30 kg / m², przy suplementacji tą samą dawką dzienną. (65) Wykazano, że wskaźnik BMI >30 kg/m² wymaga trzykrotnego zwiększenia dziennego spożycia w porównaniu do osób z normalnym wskaźnikiem masy ciała aby osiągnąć ten sam poziom witaminy.
Tym samym pacjenci z masą ciała wykazano, że indeks> 30 kg / m² wymaga trzykrotnego zwiększenia dzienne spożycie niż osoby z normalnym wskaźnikiem masy ciała osiągnąć ten sam poziom witaminy D. (27) Ponadto podczas stosowania wysokich dawek dziennych zaleca się regularne monitorowanie homeostazy mineralnej i poziomu witaminy D, jednocześnie stosowanie dawki do 4000 IU/dzień nie wymaga krótkotrwałego monitorowania.
Kolejnym ważnym wnioskiem wynikającym z niniejszego przeglądu jest to, odnotowanie faktu, iż istnieją różne klinicznie stosowane protokoły. Niektórzy autorzy badali suplementację umiarkowaną dawką dzienną, natomiast inni stosowali stosunkowo wysoką dawkę dzienną. Porównując te protokoły wydaje się, że dzienna dawka może utrzymać poziom witaminy D w pożądanym zakresie bardziej iż wysokie dawki miesięczne. Można to wytłumaczyć okresem półtrwania 25 (OH) D. Jak uprzednio wykazano okres półtrwania 25 (OH) D3 zależy od zmienności genetycznej DBP i zwykle wynosi około 15 dni. (66) Pacjenci, którzy otrzymywali 25 000 IU co dwa tygodnie przez 2 miesiące mieli niższy poziom witaminy D niż ci, którzy otrzymywali 25 000 IU tygodniowo. (36)
W innym badaniu poddano leczeniu 135 pacjentów, u których poziom witaminy wynosił D ≥ 30 ng/ ml . Pacjenci otrzymywali 50000 IU tygodniowo, przez 3 miesiące, w celu zwiększenia poziomu witaminy D z 13,2 ± 3,3 ng / ml do 37,0 ± 4,7 ng / ml. Następnie pacjenci otrzymywali dzienną dawkę 2000 IU, aby utrzymać osiągnięty poziom. Jednak po 3 miesiącach poziom witaminy D. znacznie spadła do 20,4 ± 5,4 ng / ml. Te wyniki pokazują że 2000 IU / dzień nie wystarczy do utrzymania osiągniętego, zdrowego poziomu witaminy D, nawet po terapii. (61)
Podsumowując, niniejszy przegląd zwraca uwagę na trwającą pandemię niedoboru witaminy D i podkreśla rolę witaminy D w funkcjonowaniu układu odpornościowego i jej wpływ na choroby inne niż te związane z układem kostno szkieletowym. Wyniki wykazały, że w literaturze coraz więcej jest dowodów na to, że witamina D jest ważnym czynnikiem, który może być stosowany jako terapia wspomagająca w wielu chorobach.
Jako konkluzję wykazano, że dzienna dawka witaminy D wynosząca 10 000 IU jest bezpieczna do stosowania u pacjentów współistniejących chorób wpływających na metabolizm witaminy D. Taka dzienna dawka jest często wymagana do osiągnięcia zdrowego poziom witaminy D wynoszącego 40-60 ng/ml.
INFORMACJA Z SERWISU FM DENTAL
Interesują Cię praktyczne aspekty pracy z mobilnym systemem testowym witaminy D? Masz pytania?
Nasz specjalista - Michał Sikora z przyjemnością podzieli się z Tobą swoją wiedzą i doświadczeniem.
T.: 48 882 185 520, (12) 423 49 17, E: m.sikora@fmdental.pl
Informacja o autorach
Shahram Ghanaati1, Joseph Choukroun2, Ulrich Volz3, Rebekka Hueber3, Carlos Fernando de Almeida Barros Mourão2, Robert Sader1, Yoko Kawase-Koga4, Ramesh Mazhari5, Karin Amrein6, Patrick Meybohm7, Sarah Al-Maawi1
1 Department for Oral, Cranio-Maxillofacial and Facial Plastic Surgery, Medical Center of the Goethe University Frankfurt; FORM (Frankfurt Orofacial Regenerative Medicine)-Lab, Department for Oral, Cranio-Maxillofacial and Facial Plastic Surgery, Medical Center of the Goethe University Frankfurt, Germany
2 FORM (Frankfurt Orofacial Regenerative Medicine)-Lab, Department for Oral, Cranio-Maxillofacial and Facial Plastic Surgery, Medical Center of the Goethe University Frankfurt, Germany
3 SDS Swiss Dental Solutions AG, Kreuzlingen, Switzerland
4 Department of Oral and Maxillofacial Surgery, Tokyo Women's Medical University, Tokyo, Japan
5 Division of Cardiology, George Washington University, Washington, D.C, USA
6 Department of Internal Medicine, Division of Endocrinology and Diabetology, Medical University of Graz, Graz, Austria
7 Department of Anaesthesiology, University Hospital Wuerzburg, Wuerzburg, Germany
Adres korespondencyjny:
Prof. Shahram Ghanaati
Department of Oral, Cranio-Maxillofacial and Facial Plastic Surgery, Medical Center of the Goethe University, Theodor-Stern-Kai 7, Building 23 B, UG, 60590 Frankfurt/Main
Germany
Bibliografia:
- Corzo L, Fernandez‑Novoa L, Carrera I, Martínez O, Rodríguez S, Alejo R, et al. Nutrition, health, and disease: Role of selected marine and vegetal nutraceuticals. Nutrients 2020;12:747.
- World Health Organization. “WHO Diet, Nutrition and the Prevention of Chronic Diseases. World Health Organization; 2014.
- Grünewald H. Nobel Lectures Chemistry 1901–1921 und 1922–1941. Herausgeg. von der Nobel Foundation. Elsevier Publishing Company, Amsterdam‑London‑New York 1966. Band 1901–1921: XII, 409 S., mehrere Abb., geb. Dfl. 80‑; Band 11922–1941: 536 S., mehrere Abb., geb. Dfl. 80. Angew Chemie 1968;80:52.
- Rusińska A, Płudowski P, Walczak M, Borszewska‑Kornacka MK, Bossowski A, Chlebna‑Sokół D, et al. Vitamin D supplementation guidelines for general population and groups at risk of Vitamin D deficiency in Poland‑recommendations of the polish society of pediatric endocrinology and diabetes and the expert panel with participation of national specialist consultants and representatives of scientific societies‑2018 update. Front Endocrinol (Lausanne) 2018;9:246.
- Kočovská E, Gaughran F, Krivoy A, Meier UC. Vitamin‑D deficiency as a potential environmental risk factor in multiple sclerosis, schizophrenia, and autism. Front Psychiatry 2017;8:47.
- Barnicot NA. Local action of calciferol and vitamin A on bone. Nature 1948;162:848.
- Embree ND, Ames SR, Lehman RW, Harris PL. Determination of Vitamin A. Methods Biochem Anal 1957;4:43‑98.
- Bodart F. Deficiency diseases of the bone. Wien Med Wochenschr 1950;100:584‑6.
- Gil Á, Plaza‑Diaz J, Mesa MD. Vitamin D: Classic and Novel Actions. Ann Nutr Metab 2018;72:87‑95.
- Wharton B, Bishop N. Rickets. [Review] [139 refs]. Lancet 2003 25;362:1389-400.
- Hintzpeter B, Mensink GB, Thierfelder W, Müller MJ, Scheidt‑Nave C. Vitamin D status and health correlates among German adults. Eur J Clin Nutr 2008;62:1079‑89.
- Jagelavičienė E, Vaitkevičienė I, Šilingaitė D, Šinkūnaitė E, Daugėlaitė G. The relationship between Vitamin D and periodontal pathology. Medicina (Kaunas) 2018;54:45.
- Beard JA, Bearden A, Striker R. Vitamin D and the anti‑viral state. J Clin Virol 2011;50:194‑200.
- Martineau AR, Jolliffe DA, Hooper RL, Greenberg L, Aloia JF, Bergman P, et al. Vitamin D supplementation to prevent acute respiratory tract infections: Systematic review and meta‑analysis of individual participant data. BMJ 2017;356:i6583.
- Giustina A, Adler RA, Binkley N, Bollerslev J, Bouillon R, Dawson‑Hughes B, et al. Consensus statement from 2nd International Conference on Controversies in Vitamin D. Rev Endocr Metab Disord 2020;21:89‑116.
- Amrein K, Scherkl M, Hoffmann M, Neuwersch‑Sommeregger S, Köstenberger M, Tmava Berisha A, et al. Vitamin D deficiency 2.0: An update on the current status worldwide. Eur J Clin Nutr 2020. doi: 10.1038/s41430-020-0558-y. [Epub ahead of print].
- Dobson R, Cock HR, Brex P, Giovannoni G. Vitamin D supplementation. Pract Neurol 2018;18:35‑42.
- Ferrari D, Lombardi G, Banfi G. Concerning the Vitamin D reference range: Pre‑analytical and analytical variability of Vitamin D measurement. Biochem Med (Zagreb) 2017;27:030501.
- Bikle D, Bouillon R, Thadhani R, Schoenmakers I. Vitamin D metabolites in captivity? Should we measure free or total 25(OH)D to assess Vitamin D status? J Steroid Biochem Mol Biol 2017;173:105‑16
- Grant WB, Lahore H, McDonnell SL, Baggerly CA, French CB, Aliano JL, et al., Evidence that Vitamin D Supplementation Could Reduce Risk of Influenza and COVID-19 Infections and Deaths. Nutrients 2020;12:988.
- Hu YC, Wang WW, Jiang WY, Li CQ, Guo JC, Xun YH. Low Vitamin D levels are associated with high viral loads in patients with chronic hepatitis B: A systematic review and meta‑analysis. BMC Gastroenterol 2019;19:84.
- Cashman KD, Dowling KG, Škrabáková Z, Gonzalez‑Gross M, Valtueña J, De Henauw S, et al. Vitamin D deficiency in Europe: Pandemic? Am J Clin Nutr 2016;103:1033‑44.
- German Nutrition Society. New reference values for Vitamin D Germany. Ann Nutr Metab 2012;60:241‑6.
- Bresson JL,Burlingame B, Dean T, Fairweather-Tait S, Heinonen M,Hirsch-Ernst K, et al. Scientific opinion on dietary reference values for Vitamin D. EFSA J 2016.
- Vitamin D and Health 2016 ii. 2016. Available from: https://www.gov.uk/government/groups/scientific-advisory-committee-on-nutrition
- Ross AC, Manson JE, Abrams SA, Aloia JF, Brannon PM, Clinton SK, et al. The 2011 report on dietary reference intakes for calcium and Vitamin D from the Institute of Medicine: What clinicians need to know. J Clin Endocrinol Metab 2011;96:53‑8.
- Holick MF, Binkley NC, Bischoff‑Ferrari HA, Gordon CM, Hanley DA, Heaney RP, et al. Evaluation, treatment, and prevention of Vitamin D deficiency: An Endocrine Society clinical practice guideline. J Clin Endocrinol Metab 2011;96:1911‑30.
- Adams JS, Ren S, Liu PT, Chun RF, Lagishetty V, Gombart AF, et al. Vitamin d‑directed rheostatic regulation of monocyte antibacterial responses. J Immunol 2009;182:4289‑95.
- Scientists’ Call to D*action for Public Health – Grassroots Health. Available from: https://www.grassrootshealth.net/project/our‑scientists/. [Last accessed on 2020 Mar 27].
- Vieth R. Vitamin D supplementation, 25‑hydroxyvitamin D concentrations, and safety. Am J Clin Nutr 1999;69:842‑56.
- Urashima M, Segawa T, Okazaki M, Kurihara M, Wada Y, Ida H. Randomized trial of Vitamin D supplementation to prevent seasonal influenza A in schoolchildren. Am J Clin Nutr 2010;91:1255‑60.
- Manson JE, Cook NR, Lee IM, Christen W, Bassuk SS, Mora S, et al. Vitamin D supplements and prevention of cancer and cardiovascular disease. N Engl J Med 2019;380:33‑44.
- Pittas AG, Dawson-Hughes B, Sheehan P, Ware JH, Knowler WC, Aroda VR, et al. Vitamin D supplementation and prevention of type 2 diabetes. N Engl J Med 2019;381:520‑30.
- Han JE, Jones JL, Tangpricha V, Brown MA, Brown LAS, Hao L, et al. High dose Vitamin D administration in ventilated intensive care unit patients: A pilot double blind randomized controlled trial. J Clin Transl Endocrinol 2016;4:59‑65.
- Amrein K, Schnedl C, Holl A, Riedl R, Christopher KB, Pachler C, et al. Effect of high‑dose Vitamin D3 on hospital length of stay in critically ill patients with Vitamin D deficiency: The VITdAL‑ICU randomized clinical trial. JAMA 2014;312:1520‑30.
- van Groningen L, Opdenoordt S, van Sorge A, Telting D, Giesen A, de Boer H. Cholecalciferol loading dose guideline for Vitamin D‑deficient adults. Eur J Endocrinol 2010;162:805‑11.
- Heaney RP, Davies KM, Chen TC, Holick MF, Barger‑Lux MJ. Human serum 25‑hydroxycholecalciferol response to extended oral dosing with cholecalciferol. Am J Clin Nutr 2003;77:204‑10.
- Peppone LJ, Huston AJ, Reid ME, Rosier RN, Zakharia Y, Trump DL, et al. The effect of various Vitamin D supplementation regimens in breast cancer patients. Breast Cancer Res Treat 2011;127:171‑7.
- McCullough PJ, Lehrer DS, Amend J. Daily oral dosing of Vitamin D3 using 5000 TO 50,000 international units a day in long‑term hospitalized patients: Insights from a seven year experience. J Steroid Biochem Mol Biol 2019;189:228‑39.
- Malihi Z, Lawes CMM, Wu Z, Huang Y, Waayer D, Toop L, et al. Monthly high-dose vitamin D supplementation does not increase kidney stone risk or serum calcium: Results from a randomized controlled trial. Am J Clin Nutr 2019;109:1578-7.
- Soilu-Hänninen M, Aivo J, Lindström BM, Elovaara I, Sumelahti ML, Färkkilä M, et al. A randomised, double blind, placebo controlled trial with vitamin D3 as an add on treatment to interferon β-1b in patients with multiple sclerosis. J Neurol Neurosurg Psychiatry 2012;83:565-71.
- Etemadifar M, Janghorbani M. Efficacy of high‑dose Vitamin D3 supplementation in Vitamin D deficient pregnant women with multiple sclerosis: Preliminary findings of a randomized‑controlled trial. Iran J Neurol 2015;14:67‑73.
- Howard JE, Meyer RJ. Intoxication with Vitamin D. J Clin Endocrinol Metab 1948;8:895‑910.
- Chun RF, Shieh A, Gottlieb C, Yacoubian V, Wang J, Hewison M, et al. Vitamin D binding protein and the biological activity of Vitamin D. Front Endocrinol (Lausanne) 2019;10:718.
- Dohle E, Vorakulpipat P, Al-Maawi S, Schröder R, Booms P, Sader R, et al. Effect of Vitamin D3 on nonmelanoma skin cancer cells: Acomparative in vitro study. Int J Growth Factors Stem Cells Dent 2020.
- Gholami F, Moradi G, Zareei B, Rasouli MA, Nikkhoo B, Roshani D, et al. The association between circulating 25‑hydroxyvitamin D and cardiovascular diseases: A meta‑analysis of prospective cohort studies. BMC Cardiovasc Disord 2019;19:248.
- Mirhosseini N, Vatanparast H, Kimball SM. The Association between Serum 25(OH)D Status and Blood Pressure in Participants of a Community-Based Program Taking Vitamin D Supplements. Nutrients. 2017;9. pii: E1244. doi: 10.3390/nu9111244.
- Omidian M, Mahmoudi M, Abshirini M, Eshraghian MR, Javanbakht MH, Zarei M, et al. Effects of Vitamin D supplementation on depressive symptoms in type 2 diabetes mellitus patients: Randomized placebo‑controlled double‑blind clinical trial. Diabetes Metab Syndr 2019;13:2375‑80.
- Zhu M, Wang T, Wang C, Ji Y. The association between Vitamin D and COPD risk, severity, and exacerbation: An updated systematic review and meta‑analysis. Int J Chron Obstruct Pulmon Dis 2016;11:2597‑607.
- Heidari B, Hajian‑Tilaki K, Babaei M. Vitamin D deficiency and rheumatoid arthritis: epidemiological, immunological, clinical and therapeutic aspects. Mediterr J Rheumatol 2019;30:94‑102.
- Feige J, Moser T, Bieler L, Schwenker K, Hauer L, Sellner J. Vitamin D Supplementation in Multiple Sclerosis: A Critical Analysis of Potentials and Threats. Nutrients 2020;12. pii: E783. doi: 10.3390/nu12030783.
- Borella E, Nesher G, Israeli E, Shoenfeld Y. Vitamin D: A new anti‑infective agent? Ann N Y Acad Sci 2014;1317:76‑83.
- Fan HZ, Zhang R, Tian T, Zhong YL, Wu MP, Xie CN, et al. CYP24A1 genetic variants in the Vitamin D metabolic pathway are involved in the outcomes of hepatitis C virus infection among high‑risk Chinese population. Int J Infect Dis 2019;84:80‑8.
- Brice DC, Toth Z, Diamond G. LL‑37 disrupts the Kaposi’s sarcoma‑associated herpesvirus envelope and inhibits infection in oral epithelial cells. Antiviral Res 2018;158:25‑33.
- Alvarez N, Aguilar‑Jimenez W, Rugeles MT. The potential protective role of Vitamin D supplementation on HIV‑1 infection. Front Immunol 2019;10:2291.
- Giraldo DM, Cardona A, Urcuqui‑Inchima S. High‑dose of Vitamin D supplement is associated with reduced susceptibility of monocyte‑derived macrophages to dengue virus infection and pro‑inflammatory cytokine production: An exploratory study. Clin Chim Acta 2018;478:140‑51.
- Arboleda JF, Urcuqui‑Inchima S. Vitamin D‑regulated microRNAs: Are they protective factors against dengue virus infection? Adv Virol 2016;2016:1016840.
- Lu D, Zhang J, Ma C, Yue Y, Zou Z, Yu C, et al. Link between community‑acquired pneumonia and Vitamin D levels in older patients. Z Gerontol Geriatr 2018;51:435‑9.
- Laplana M, Royo JL, Fibla J. Vitamin D Receptor polymorphisms and risk of enveloped virus infection: A meta‑analysis. Gene 2018;678:384‑94.
- Sanders KM, Stuart AL, Williamson EJ, Simpson JA, Kotowicz MA, Young D, et al. Annual high‑dose oral Vitamin D and falls and fractures in older women: A randomized controlled trial. JAMA 2010;303:1815‑22.
- Sadat‑Ali M, Al‑Anii FM, Al‑Turki HA, AlBadran AA, AlShammari SM. Maintenance dose of Vitamin D: How much is enough? J Bone Metab 2018;25:161‑4.
- Araki T, Holick MF, Alfonso BD, Charlap E, Romero CM, Rizk D, et al. Vitamin D intoxication with severe hypercalcemia due to manufacturing and labeling errors of two dietary supplements made in the United States. J Clin Endocrinol Metab 2011;96:3603‑8.
- Koutkia P, Chen TC, Holick MF. Vitamin D intoxication associated with an over‑the‑counter supplement. N Engl J Med 2001;345:66‑7.
- Jacobus CH, Holick MF, Shao Q, Chen TC, Holm IA, Kolodny JM, et al. Hypervitaminosis D associated with drinking milk. N Engl J Med 1992;326:1173‑7.
- Ekwaru JP, Zwicker JD, Holick MF, Giovannucci E, Veugelers PJ. The importance of body weight for the dose response relationship of oral Vitamin D supplementation and serum 25‑hydroxyvitamin D in healthy volunteers. PLoS One 2014;9:e111265.
- Jones KS, Assar S, Harnpanich D, Bouillon R, Lambrechts D, Prentice A, et al. 25(OH) D2 half‑life is shorter than 25(OH)D3 half‑life and is influenced by DBP concentration and genotype. J Clin Endocrinol Metab 2014;99:3373‑81.


